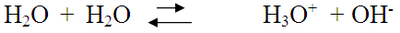Nell’acqua allo stato liquido uno dei due atomi di idrogeno mostra una leggerissima tendenza a rompere il legame covalente che lo lega all’ossigeno e a passare su una seconda molecola di acqua.

Questa reazione, detta di autoprotolisi dell’acqua, porta alla formazione di due ioni:
- ione ossonio o idronio H3O+
- ione ossidrile OH-
In realtà, nell’acqua pura questo fenomeno si verifica solo per una molecola su più di cinquecento milioni di molecole. Inoltre è un fenomeno dinamico: cioè per un dato numero di molecole che si ionizzano, c’è un numero identico di molecole che si riassociano, per cui la loro quantità per unità di volume, cioè la loro concentrazione, rimane costante.
In pratica siamo di fronte a quello che in chimica viene definito equilibrio dinamico.
Possiamo quindi descriverlo così:
Nella forma più corretta:
Le due frecce stanno ad indicare che la reazione avviene in entrambi i sensi. Quella che punta verso sinistra è più lunga e ciò sta ad indicare che è la reazione favorita, cioè in condizioni normali avremo pochissime molecole di acqua che si ionizzano.
Per facilità di esposizione e di calcolo indicheremo lo ione idrogeno al posto dello ione idronio.
Quindi possiamo affermare che nell’acqua pura il numero di ioni H+ è uguale al numero di ioni OH-.
Secondo una legge chimica (legge dell’equilibrio mobile) il prodotto della concentrazione degli ioni H+ e di quella degli ioni OH- è costante, a temperatura costante (25°C).
Se però nell’acqua aggiungiamo sostanze che si dissociano e per effetto di questa dissociazione producono ioni H+ oppure ioni OH-, la situazione che si viene a creare è diversa da quella che si presenta nell’acqua pura.
Se ad esempio aggiungiamo l’acido cloridrico all’acqua, questa sostanza si dissocia liberando ioni H+ e ioni Cl- in grande quantità.
Se invece aggiungiamo l’idrossido di sodio all’acqua, esso si ionizzerà liberando ioni Na+ e ioni OH- in grande quantità.
In chimica le sostanze che si comportano come l’acido cloridrico, che fanno quindi aumentare la concentrazione di ioni idrogeno, vengono dette acidi, quelle che si comportano come l’idrossido di sodio, cioè quelle che fanno aumentare la concentrazione di ioni ossidrile, vengono dette basi o alcali.
L’acido cloridrico e l’idrossido di sodio si ionizzano completamente in acqua: per questa loro caratteristica vengono detti forti.
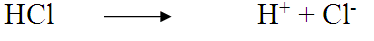
Acido cloridrico (acido forte: si ionizza completamente)

Idrossido di sodio (base forte: si ionizza completamente)
Altri invece possono ionizzarsi solo in parte; in questo caso vengono detti deboli, dato che fanno aumentare di poco la concentrazione degli ioni H+ oppure OH-.
Acido etanoico o acetico (acido debole: si dissocia parzialmente)
Idrossido di magnesio (base debole: si dissocia parzialmente)
Per definire il grado di acidità di una soluzione si usa il pH (dal tedesco potenz Hydrogen, cioè potere dell’idrogeno). È stata costruita una scala di pH, che è una misura della concentrazione dello ione idrogeno in soluzione; essa va da 0 a 14.
Un pH di 7 indica che la soluzione è neutra e quindi si ha una concentrazione uguale di ioni H+ e OH-, per cui essi si bilanciano e si verifica quindi la stessa situazione dell’acqua pura. Per valori di pH minori di 7, il valore di ioni H+ in soluzione aumenta mentre quello degli ioni OH- diminuisce: si parla di pH acido. Un valore maggiore di 7 indica invece una diminuzione di ioni H+ e quindi un aumento di ioni OH-.
Schematizzando
pH < 7 → concentrazione di ioni H+ > concentrazione di ioni OH- → soluzione acida
pH = 7 → concentrazione di ioni H+ = concentrazione di ioni OH- → soluzione neutra
pH > 7 → concentrazione di ioni H+ < concentrazione di ioni OH- → soluzione basica o alcalina
Bisogna tener conto del fatto che alla variazione di una unità di scala del pH corrisponde la variazione di 10 volte, quindi un ordine di grandezza, nella concentrazione di ioni H+. In pratica se passiamo dal pH 6 al pH 5, vuol dire che la concentrazione di ioni idrogeno è aumentata di 10 volte.
Fonti
H. Curtis - N.S. Barnes - Invito alla biologia - Zanichelli Editore (quarta edizione italiana)