Il momento dipolare misura la polarità di un legame chimico. Viene indicato con μ e vale:
μ = δ•d
dove δ è la carica mentre d rappresenta la distanza di legame.
L’unità SI del momento dipolare è il coulomb•metro ma spesso si misura debye (D) che è un’unità più piccola, più utile quando si studiano i deboli dipoli delle molecole.
1 C•m = 2,9979•1029 D
Il momento dipolare si rappresenta con un vettore (dato che è una grandezza vettoriale) “particolare”, parallelo all’asse di legame, con la freccia che va dall’atomo meno elettronegativo verso quello più elettronegativo. Si mette quella specie di segno + per indicare che il vettore è nella direzione contraria a quella convenzionale.

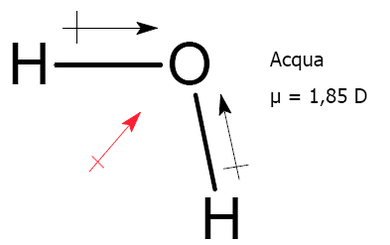
Qui ovviamente entra in gioco anche la geometria molecolare. Ad esempio sia la formaldeide che l’anidride carbonica contengono un gruppo carbonilico C=O: se si misura sperimentalmente il momento dipolare di entrambe le molecole si vede che la prima è altamente polare mentre la seconda non lo è. Questo si verifica grazie al fatto che la CO2 è una molecola lineare e quindi ciascun dipolo annulla l’altro.
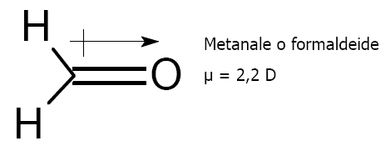

Per farvi comprendere bene l’importanza della simmetria, utilizzerò dei composti che derivano formalmente dal metano, in cui, uno alla volta, sostituirò un atomo di idrogeno con uno di cloro.
Tutti questi composti contengono legami polari di tipo C-Cl, ma nel CCl4 la simmetria del carbonio tetraedrico tende a cancellare i dipoli, conferendo alla molecola l’apolarità.
Nelle figure seguenti, in bianco sono rappresentati gli atomi di idrogeno, in celeste il carbonio e in verde il cloro.

Clorometano CH3Cl: la molecola mostra un momento dipolare di 1,87 D.

Diclorometano CH2Cl2: la molecola mostra un momento dipolare di 1,54 D.

Triclorometano CHCl3 (cloroformio): la molecola mostra un momento dipolare di 1,02 D.

Tetraclorometano CCl4 (tetracloruro di carbonio): la molecola mostra un momento dipolare nullo (μ = 0 D).
Se volete, potete scaricare la lezione in formato pdf:
