A differenza di glucidi e lipidi (che di regola non contengono azoto), le proteine sono composti organici quaternari, che possiedono sempre atomi di azoto nella loro molecola (quasi sempre anche atomi di zolfo; spesso fosforo e talvolta atomi metallici: ferro, zinco, rame...).
Il ruolo primario che le proteine svolgono nei sistemi viventi è dichiarato dal loro stesso nome (che deriva dal greco protéion cioè "primato"). Sono le molecole organiche più complesse, più importanti e più "personalizzate" che si ritrovino in un organismo. Anche quantitativamente sono le prime: più del 50% di tutto il materiale organico di una cellula vivente è fatto di proteine. Possono avere nell'organismo una funzione energetica, come i glucidi e i lipidi; ma essa è del tutto secondaria rispetto a due altri ruoli: quello strutturale, di "materiali da costruzione", e quello di "utensili" ( = enzimi) indispensabili per montare, smontare e trasformare altre molecole.
Chimicamente, le proteine sono polimeri, come i polisaccaridi. Le loro subunità sono dette aminoacidi; la figura qui sotto mostra la loro struttura fondamentale:
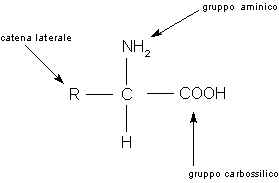
Come si vede, un atomo centrale di carbonio lega contemporaneamente:
- un gruppo amminico (basico) -NH2
- un gruppo carbossilico (acido) -COOH
- un atomo di idrogeno
- una restante porzione della molecola (detta catena laterale e indicata genericamente con R), che ha una composizione chimica variabile dall'uno all'altro aminoacido.
L'atomo di carbonio al centro viene detto carbonio alfa. Ogni subunità proteica (=aminoacido) possiede dunque almeno un atomo di azoto (altri possono essere contenuti nelle catene laterali R).
Complessivamente sono stati identificati nelle proteine 20 tipi di aminoacidi, diversi l'uno dall'altro per struttura e composizione della catena laterale.
Molte altre varietà di aminoacidi (più di 150!) si possono ancora ritrovare nelle cellule viventi, non però come costituenti di proteine, bensì come molecole singole, incaricate di funzioni particolari.
L'unione in catena degli aminoacidi avviene mediante un legame peptidico:

che si stabilisce tra il gruppo carbossilico di ciascuno e il gruppo aminico del successivo:

La catena (polipeptide) può allungarsi fino a comprendere anche centinaia di aminoacidi. Le molecole delle proteine sono formate, a seconda dei casi, da una catena polipeptidica unica, oppure da due o più catene strettamente associate tra loro, e spesso unite da legami trasversali di varia natura (ad esempio ponti ad idrogeno, oppure ponti disolfuro -S-S- tesi tra coppie di atomi di zolfo).
Nella struttura di una proteina si riconoscono vari livelli
Una parola è formata da un gruppo di lettere allineate, in una certa sequenza, su un unico piano: il foglio di carta. Invece gli aminoacidi che compongono una proteina non giacciono tutti nello stesso piano: la loro sequenza costruisce un "nastro" che assume certe pieghe (cioè una certa disposizione tridimensionale) e che, combinandosi con altri nastri ( = altre catene polipeptidiche), può generare strutture ancora più elaborate: trecce, matasse, foglietti variamente pieghettati...
Il modo in cui si dispongono nello spazio le catene polipeptidiche (quindi la forma complessiva assunta dalla molecola proteica) è altrettanto importante quanto la corretta sequenza dei singoli aminoacidi, per garantire il funzionamento di una proteina. Una prova di ciò è fornita dal fenomeno della denaturazione da calore, che già conosciamo: esso si limita a scompigliare la forma di una molecola proteica, senza spezzare o alterare i legami peptidici (robusti, perché covalenti) che uniscono i singoli aminoacidi; e tuttavia causa la perdita delle proprietà e delle funzioni che erano caratteristiche di quella proteina.
Per descrivere esaurientemente una molecola proteica occorre dunque precisarne:
- la struttura primaria, cioè la sequenza dei singoli aminoacidi che compongono quella molecola;
- la struttura secondaria, cioè il tipo di "nastro" originato dalla catena polipeptidica: irregolarmente disteso, oppure avvolto ad "alfa elica" (come le spire regolari di una molla cilindrica), o ancora pieghettato a zig zag, secondo uno schema detto "lamina beta" o "beta-foglietto";
- la struttura terziaria, cioè la forma complessiva che il nastro di aminoacidi conferisce alla proteina fibrosa, oppure globulare (quando il nastro si ripiega più volte su se stesso, a formare una aggrovigliata matassa).
- Infine, se la proteina è costituita non da un'unica catena polipeptidica, bensì da due o più, allora bisognerà ancora precisarne la struttura quaternaria, cioè il modo in cui ciascuna catena si affianca o si intreccia alle compagne.


Non solo esistono proteine fatte di più catene polipeptidiche, ma anche strutture formate dalla riunione di molte molecole proteiche. Sono i complessi proteici sopramolecolari, che raggiungono dimensioni tali da poter essere agevolmente osservati al microscopio elettronico, al quale rivelano le loro regolari ed eleganti geometrie. Esempi di questi complessi sono le robuste fibrine di collagene (presenti ad esempio nei tendini), o gli involucri proteici dei virus.
Numerose proteine, quando vengono "smontate" per studiarne la composizione, rivelano di contenere non soltanto aminoacidi, ma anche altri componenti, inorganici (per esempio metalli come il ferro, il rame, lo zinco) oppure organici (lipidi, glucidi...). Perciò i biochimici distinguono due categorie di proteine: quelle semplici (fatte soltanto di aminoacidi) e quelle coniugate, che contengono un gruppo prostetico (dal greco prósthesis, "aggiunta") di natura non aminoacidica. Sono esempi della seconda categoria: le lipoproteine e le glicoproteine di cui è ricco il sangue, le fosfoproteine che possiamo ritrovare nel latte o nel tuorlo d'uovo, e le emoproteine, quale l'emoglobina dei globuli rossi.
L'eccezionale versatilità delle proteine rende difficile illustrare in modo breve ma esauriente tutti i compiti che esse possono svolgere in un organismo. Schematicamente, possiamo riconoscere che esistono i seguenti tipi.
Proteine di deposito, funzionanti come molecole-magazzino di materiali utili.
Un esempio di questo tipo è la ferritina, proteina alla quale viene agganciato, perché non sia eliminato dal corpo, tutto il ferro che la milza recupera dalla "demolizione" dei globuli rossi vecchi. Altre proteine di deposito servono come riserve di aminoacidi per un embrione in sviluppo (pensate al tuorlo d'uovo, o alle riserve proteiche che abbondano nei semi delle piante); oppure come cibo "nobile" per un piccolo essere ancora incapace di alimentazione autonoma (pensate alla caseina del latte, nei mammiferi).
Proteine strutturali, fibrose e insolubili, alle quali gli organismi animali affidano la funzione di dar forma e sostegno a tutto il corpo, funzione che nei vegetali è svolta soprattutto dai polisaccaridi.
Il collagene di ossa, tendini e tessuti connettivi, la cheratina della pelle e l'elastina dei polmoni e dei vasi sanguigni sono esempi di queste proteine.
Proteine catalitiche.
Si tratta di molecole-utensili per la trasformazione di altre molecole; tutti gli enzimi rientrano in questa categoria.
Proteine contrattili.
Sono l'actina e la miosina, che permettono ai muscoli di accorciarsi e di compiere lavoro meccanico.
Proteine di trasporto.
Ad esempio l'emoglobina, che nei globuli rossi dei vertebrati è "veicolo" dei gas respiratori; o le lipoproteine, che trasportano nel plasma sanguigno i grassi, altrimenti insolubili.
Proteine inserite nelle membrane cellulari, con il compito di permettere e regolare flussi di sostanze tra le cellule e l'ambiente esterno.
Proteine messaggere.
Si tratta di proteine che recano ai vari organi del corpo segnali capaci di influenzarne l'attività, sono di questo tipo gli ormoni proteici dei vertebrati.
Raccolta di materiale di biologia effettuata con la classe 3a A st nell'anno scolastico 1999/2000 - ITIS V. Volterra di Ancona
